特效新药: FDA批准首个对成年多发性骨髓瘤患者的基因治疗
2021年3月27日美国食品和药物管理局批准了Abecma(idecabtagene vicleucel),这是一种基于细胞的基因疗法,可用于治疗多发性骨髓瘤的成年患者,这些患者对至少四项先前的治疗方法(不同类型)无反应或在治疗后已复发。Abecma是FDA批准的首个基于细胞的基因疗法,可用于治疗多发性骨髓瘤。
FDA的生物制品评估与研究中心主任Peter Marks博士说:“ FDA仍致力于为患者未满足的需求领域提供新颖的治疗选择。虽然无法治愈多发性骨髓瘤,但长期前景可能会因患者的年龄和诊断时的病情阶段而异。今天的批准为患有这种罕见癌症的患者提供了一种新的治疗选择。”
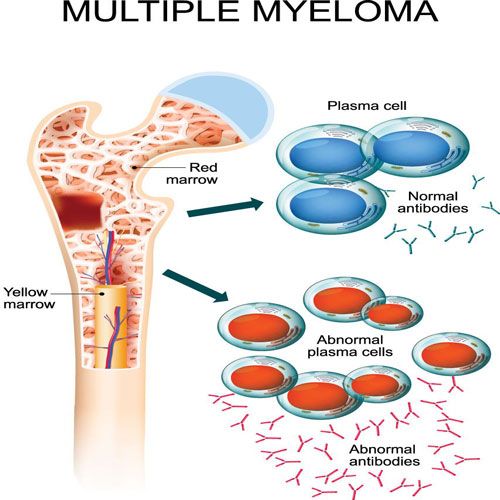
多发性骨髓瘤是一种罕见的血液癌,其中异常浆细胞在骨髓中积累并在人体许多骨骼中形成肿瘤。这种疾病使骨髓无法产生足够的健康血细胞,从而导致血液计数降低。骨髓瘤还会损害骨骼和肾脏,并削弱免疫系统。多发性骨髓瘤的确切原因尚不清楚。根据2020年国家癌症研究所外部链接免责声明,骨髓瘤约占美国所有新癌症病例的1.8%(约32,000)。
Abecma是一种B细胞成熟抗原(BCMA)指导的基因修饰的自体嵌合抗原受体(CAR)T细胞疗法。每剂量的阿贝卡玛都是一种定制疗法,通过使用患者自己的T细胞(一种白细胞)创造出来,以帮助对抗骨髓瘤。收集患者的T细胞并进行基因修饰,使其包含有助于靶向和杀死骨髓瘤细胞的新基因。一旦细胞被修饰,它们便被注入患者体内。
Abecma的安全性和有效性在一项针对多发性骨髓瘤(完成治疗后复发的骨髓瘤)和难治性骨髓瘤(对治疗无反应的骨髓瘤)的127例患者的多中心研究中确定,这些患者至少接受过3种先前的抗骨髓瘤治疗。研究组中约88%的患者曾接受过4种或更多种抗骨髓瘤治疗。总体而言,有72%的患者对治疗有部分或完全反应。在接受研究的患者中,有28%的患者对Abecma表现出完全缓解(或多发性骨髓瘤的所有体征消失),并且该组中有65%的患者对治疗完全缓解了至少12个月。
用阿贝玛治疗可能会导致严重的副作用包括:噬血细胞淋巴组织细胞增生症/巨噬细胞活化综合征(HLH / MAS),神经系统毒性和血细胞减少症,这些都可能致命或危及生命。 CRS和HLH / MAS是对CAR-T细胞活化和增殖的全身反应,引起高烧和流感样症状,而长时间的血细胞减少症是某些血细胞类型数量在长时间内下降。
Abecma最常见的副作用包括CRS,感染,疲劳,肌肉骨骼疼痛和免疫系统减弱。治疗后的副作用通常会在治疗后的前一到两周内出现,但某些副作用可能会在以后发生。多发性骨髓瘤患者应咨询其医疗保健专业人员,以确定Abecma是否适合他们。
由于存在CRS和神经毒性的风险,正在批准Abecma进行风险评估和缓解策略,其中包括确保安全使用的要素。FDA要求分配Abecma的医院及其相关诊所必须经过特殊认证,并且参与处方,配药或管理Abecma的工作人员必须接受培训,以识别和管理CRS和神经系统毒性以及Abecma的其他副作用。另外,必须告知患者潜在的严重副作用,以及如果在接受Abecma后出现副作用,立即返回治疗部位的重要性。
为了进一步评估长期安全性,FDA还要求制造商进行上市后观察研究,其中涉及接受Abecma治疗的患者。
(原创)美国希望之光医疗编译,欢迎转载,请注明出处。

全球顶级医生协会(Global Top Doctors Association)是美国加州政府正式注册的联邦政府批准的一个非营利性,非宗教,非政治性国际社会组织,总部位于洛杉矶。全球顶级医生协会为中西方医学和精神专业人士的科学研究创造更有利的环境,为他们提供机会在社区,全国以及全球服务人群,满足民众的身体与精神健康需求。

