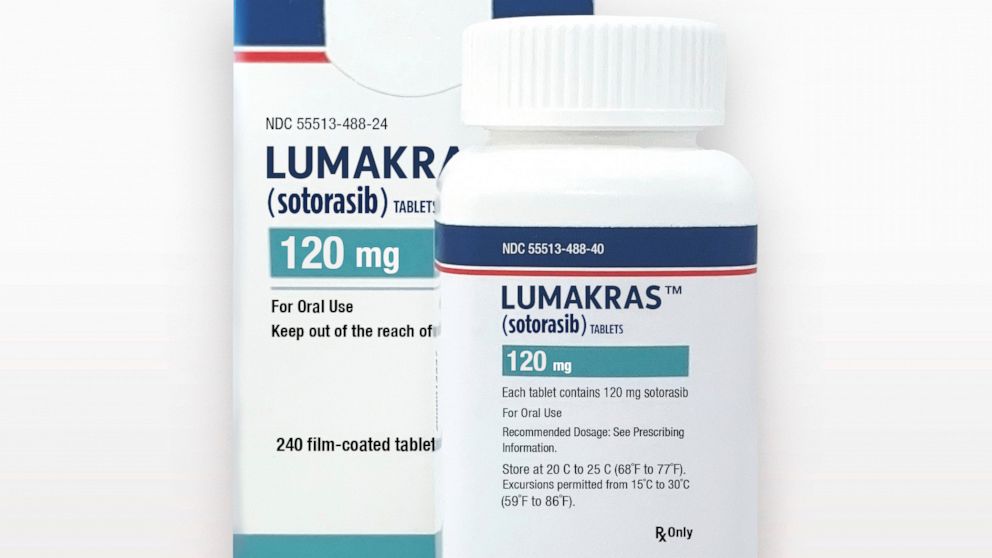
2021年5月28日美国食品和药物管理局批准Lumakras(sotorasib索托拉西)作为第一种治疗成人非小细胞肺癌患者的药物,这些患者的肿瘤具有称为KRAS G12C的特定类型的基因突变,并且之前至少接受过一种全身治疗。这是第一个获批的针对具有任何KRAS 突变的肿瘤的靶向治疗,KRAS突变约占非小细胞肺癌突变的25%。 KRAS G12C 突变约占非小细胞肺癌突变的13%。
FDA 肿瘤学卓越中心主任兼肿瘤疾病办公室代理主任理查德·帕兹杜尔 (Richard Pazdur) 说,“长期以来,KRAS 突变一直被认为对药物治疗具有抗性,这代表了某些类型癌症患者真正未满足的需求。”
肺癌是死亡率最高的最常见的癌症类型,在很大程度上可以根据导致它的基因突变进行分类。KRAS是一组有助于调节细胞生长和分裂的基因中的一种突变。
研究人员在一项对124名局部晚期或转移性KRAS G12C 突变非小细胞肺癌患者接受免疫检查点抑制剂和/或铂类化疗后疾病进展的研究中评估了Lumakras的疗效。测量的主要结果是客观反应率(肿瘤被破坏或缩小的患者比例)和反应持续时间。客观反应率为36%,其中58%的患者反应持续时间为6个月或更长时间。
Lumakras最常见的副作用:包括腹泻、肌肉骨骼疼痛、恶心、疲劳、肝损伤和咳嗽。如果患者出现间质性肺病的症状,应停用Lumakras,如果确诊为间质性肺病,则应永久停用Lumakras。
Lumakras(sotorasib索托拉西 )口服片剂含量和价格:240片(瓶) 120MG,大约为21,186美元。
医疗保健专业人员应在开始和服用Lumakras之前监测患者的肝功能测试。如果患者出现肝损伤,应停用Lumakras、减少剂量或永久停药。患者在服用Lumakras时应避免服用减酸剂、诱导或作为肝脏中某些酶的底物的药物以及作为 P-糖蛋白底物的药物。

(原创)美国希望之光医疗编译,欢迎转载,请注明出处。
全球顶级医生协会(Global Top Doctors Association)是美国加州政府正式注册的联邦政府批准的一个非营利性,非宗教,非政治性国际社会组织,总部位于洛杉矶。全球顶级医生协会为中西方医学和精神专业人士的科学研究创造更有利的环境,为他们提供机会在社区,全国以及全球服务人群,满足民众的身体与精神健康需求。

