2020年6月29日美国食品和药物管理局批准Keytruda(pembrolizumab)进行静脉注射,用于不可切除或转移性微卫星不稳定性高(MSI-H)或错配修复缺陷型(dMMR)大肠癌的一线治疗。这标志着该患者人群不需与化疗联用,这是首个治疗该患者群体一线免疫疗法。
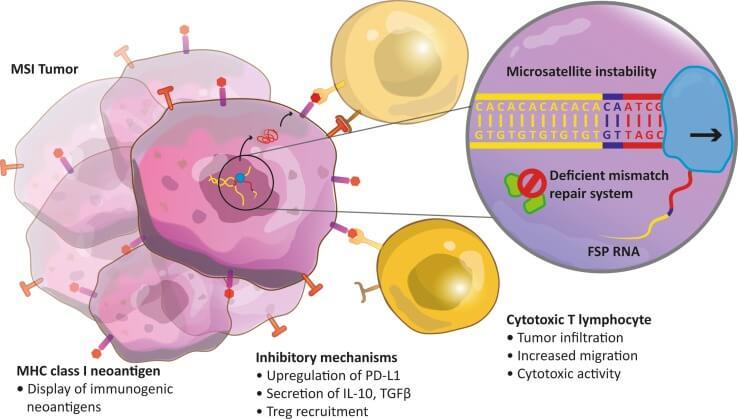
MSI-H和dMMR肿瘤包含影响细胞内DNA正确修复的异常。 MSI-H的频率随肿瘤类型和阶段而异,大约5%的转移性结直肠癌患者患有MSI-H或dMMR肿瘤。
FDA药物评估和研究中心肿瘤病学办公室代理主任Richard Pazdur医师表示,“转移性大肠癌是一种严重且威胁生命的疾病,预后很差。目前可用的化学疗法联合化疗和其他生物制剂疗法均会带来严重的毒性。”
Keytruda的作用是针对人体免疫细胞和某些癌细胞上的蛋白质PD-1 / PD-L1的细胞途径。通过阻止这种途径,Keytruda可以帮助人体的免疫系统抵抗癌细胞,并为MSI-H或dMMR转移性结直肠癌患者带来益处。
FDA先前已批准Keytruda治疗其他类型的癌症。
FDA对这一适应症的批准基于一项多中心,国际,开放标签,主动控制,随机试验的结果,该试验比较了Keytruda与307例MSI-H或dMMR转移性结直肠癌患者的化疗治疗。
通过盲法独立审查评估,该研究表明无进展生存期(PFS)有统计学显着改善。Keytruda组的中位PFS为16.5个月,标准护理组的中位PFS为8.2个月。需要进行长期分析以评估对生存的影响。
Keytruda的常见副作用包括疲劳,肌肉骨骼疼痛,食欲下降,皮肤瘙痒(瘙痒),腹泻,恶心,皮疹,发烧(发热),咳嗽,呼吸困难(呼吸困难),便秘,疼痛和腹痛。
Keytruda可引起称为免疫介导的副作用的严重状况,包括健康器官的炎症,例如肺部(肺炎),结肠(结肠炎),肝脏(肝炎),内分泌腺体(内分泌病变)和肾脏(肾炎)。严重或危及生命的输注相关反应的患者应停止服用Keytruda。
Keytruda可能会对孕妇发育中的胎儿造成伤害。母乳喂养的妇女不应服用Keytruda,因为它可能会对母乳喂养的孩子造成伤害。
Keytruda1小瓶100mg / 4ml 在美国的价格大约为9600美元。
(原创)美国希望之光医疗编译,欢迎转载,请注明出处。

全球顶级医生协会(Global Top Doctors Association)是美国加州政府正式注册的联邦政府批准的一个非营利性,非宗教,非政治性国际社会组织,总部位于洛杉矶。全球顶级医生协会为中西方医学和精神专业人士的科学研究创造更有利的环境,为他们提供机会在社区,全国以及全球服务人群,满足民众的身体与精神健康需求。

